ChonBlock™: ELISAにおける偽陽性/偽陰性反応の解決策
- 更新情報1:
ヒト血清サンプルを用いて測定する際にChonBlock™が測定結果を改善し、より正確なデータに繋がることを実証する、査読付きオープンアクセス論文を発表しました。
Kuniaki Terato, Christopher T. Do, Dawn Cutler, Takaki Waritani, Hiroshi Shionoya(2014), Preventing intense false positive and negative reactions attributed to the principle of ELISA to re-investigate antibody studies in autoimmune diseases. J Immunol Methods: https://doi.org/10.1016/j.jim.2014.03.013 - 更新情報2:
ChonBlock™を用いてヒト血清サンプルを測定するための詳細なプロトコルを提供する査読付きオープンアクセス論文を発表しました。
Takaki Waritani, Jessica Chang, Bonnie McKinney, Kuniaki Terato(2017), An ELISA protocol to improve the accuracy and reliability of serological antibody assays. MethodsX: https://doi.org/10.1016/j.mex.2017.03.002
生体試料中の特異抗原に対する抗体量を測定する酵素免疫吸着測定法(ELISA)は、40年近く前に発明されて以来、科学研究の中心的な存在となっており、種々の疾患を有する患者血清中の自己由来成分や病原体成分に対する抗体の検出に活用できます。PubMedで「ELISA」というキーワードで検索すると、この方法を用いた分析研究や臨床研究の論文が驚くほど多く出てきます。その中でも一般的に用いられている手法の一つが間接ELISA法であり、以下にその概要を示します。
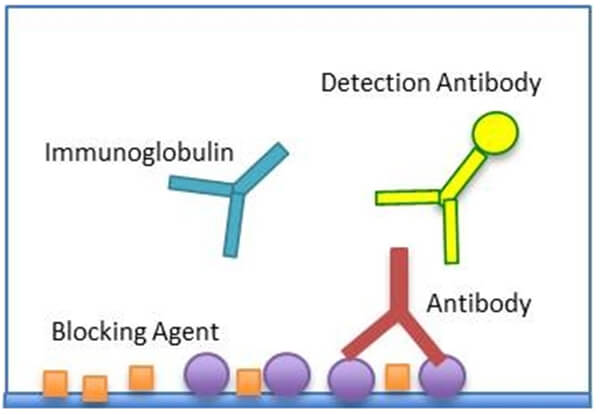
- 抗原は疎水結合により、ELISAプレートのプラスチック表面に固定化されます
- 残りの結合部位はブロッキング剤で飽和されます
- 試料中の抗原特異的抗体は固定化抗原に結合し、固定化抗原に特異的でない免疫グロブリンは洗い流されます
- コーティングされた抗原に結合した抗体を酵素標識検出抗体で検出します
- 発色は発色基質を用いて行います
間接ELISA法以外の方式(ダイレクトELISA、サンドイッチELISA、競合ELISAなど)では検出方法が異なりますが、基本的な原理は同じで、タンパク質とプラスチック表面との結合親和性が高いことを利用しております。しかし、この原理は様々な非特異的反応を引き起こし、結果の誤認やデータの誤解を招く原因となります。
以下に、間接ELISA法による抗体アッセイにおいて、誤検出の原因となる非特異的反応のうち、主な4つの非特異的反応を紹介します。
1. 試料中の免疫グロブリンとELISAプレートとの疎水性結合
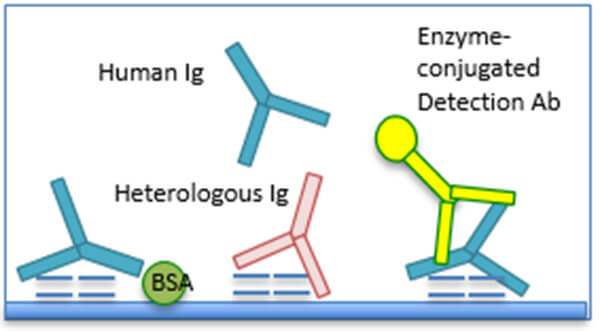
検体中の免疫グロブリンは疎水性相互作用を介してELISAプレートのプラスチック表面に強く結合します。現在のところ、Fujiiら(1989)により報告されたプラスチック表面に競合的に結合する異種血清中の免疫グロブリンを除いて、この相互作用を効果的にブロックすることのできるブロッキング剤は存在しません。プラスチック表面に結合した免疫グロブリンは、抗原に結合した特異的抗体とともに、二次抗体によって検出されます。この反応はバックグラウンドノイズ反応と呼ばれ、個々のサンプルに固有の反応であり、間接ELISAにおいて最も重大な偽陽性反応となります。この反応は各サンプルについてコントロール用の非コーティングウェルを用意し、コーティングウェルのサンプルOD値からコントロールOD値を差し引くことで説明することができます。しかし、このステップはしばしば省略されており、結果的に混乱を招いております。
2. イオン結合と特異的タンパク質相互作用による免疫グロブリンの抗原への非特異的結合
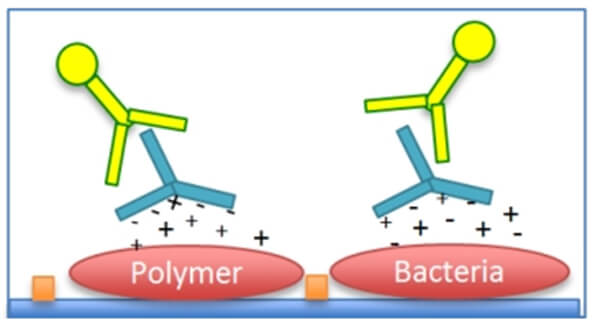
免疫グロブリンは高電荷を帯びた高分子抗原や粒子抗原に結合します。
例えば以下のようなものがあります。
- 免疫グロブリンのポリ-L-リジンへの強いイオン結合
- 免疫グロブリンの細菌粒子への非特異的結合
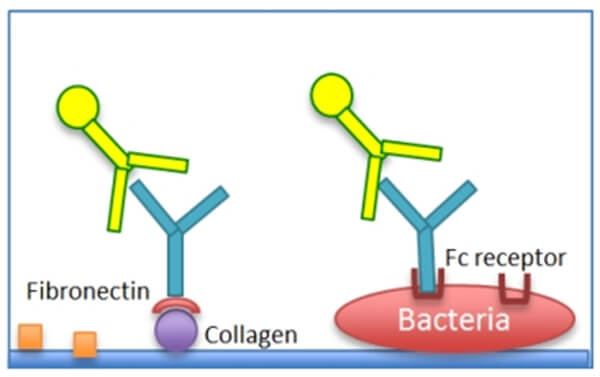
高分子量の抗原と免疫グロブリン間のような強い、特異的または非特異的なタンパク質-タンパク質相互作用は、免疫グロブリンが標的抗原に直接または間接的に結合し、結果としてサンプル中の評価対象物の過大評価に繋がる可能性があります。
例えば以下のようなものがあります。
- 免疫グロブリン-フィブロネクチン、フィブロネクチン-コラーゲン、フィブロネクチン-細菌、IgG-IgG Fc受容体、
および細菌細胞壁上のIgG-Protein A
3. 検体中の自然抗体のブロッキング剤や混入物質との結合
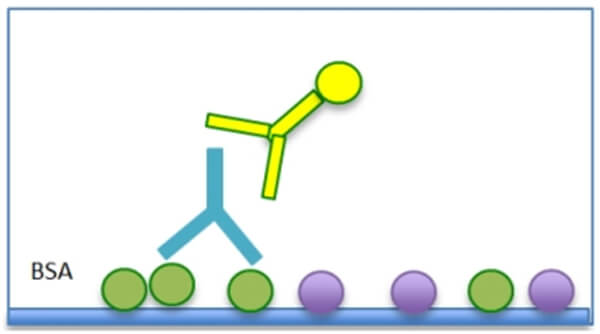
ヒトおよび動物は、食物由来のタンパク質や病原体を含む、一生のうちに曝露される全ての環境物質に対する抗体を保有しています。結果的に、これらの自然抗体はBSA(食事性タンパク質)、カゼイン(食事性タンパク質)、および異種血清成分(および抗原調製物中の混入物質)などのブロッキング剤と強く反応して、間接ELISAにおいて様々な偽陽性反応を引き起こします。
4. 検出抗体のプラスチック表面や抗原への非特異的結合
サンプル中の免疫グロブリンと同様に、評価対象物の濃度を可視化するために使用する検出抗体もプラスチック表面や抗原分子に非特異的に結合します。この非特異的な結合は、ブランクウェル中で決定することができ、使用される検出抗体の濃度は非常に低い(ng~µg/mL)ため、一般的にバックグラウンドノイズ反応よりもはるかに低いです。しかし、検出抗体は細菌やコラーゲンなどの特定の抗原に付着し、異常に高いブランク値を示すことがあるので注意が必要です。
ELISA法は非常に多くの論文が参照されていることから、数十年に渡って医学研究の発展に貢献してきたことがわかります。このような大量のデータがELISA法に依存していることを考えると、現在のELISA法のフォーマットを再評価し、その原理に起因する反応の複雑さを認識することが重要であると考えます。このような非特異的反応を排除することは、抗体濃度が低い場合の感染症の診断やワクチンの有効性を評価する上で特に重要です。
Chondrex社の提案
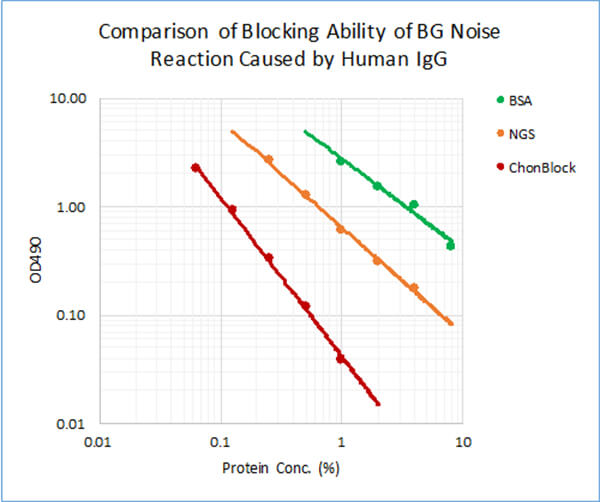
2014年にChondrex社の研究者によって行われた研究では、従来のELISAバッファーシステムと新しいELISAバッファーシステムであるChonBlock™によるこれらの偽陽性反応のブロッキング効果を比較しました。最も強い偽陽性反応を阻止するという点では、ChonBlock™は他のバッファーシステムと比較して、サンプル中の免疫グロブリンのプラスチック表面への疎水結合をより効果的に阻止しました。(下図参照)
さらに、ChonBlock™は、免疫グロブリンと抗原間のイオン性およびタンパク質-タンパク質相互作用を防ぐことができることが証明されました。
Kuniaki Terato, Christopher T. Do, Dawn Cutler, Takaki Waritani, Hiroshi Shionoya(2014), Preventing intense false positive and negative reactions attributed to the principle of ELISA to re-investigate antibody studies in autoimmune diseases.
J Immunol Methods: https://doi.org/10.1016/j.jim.2014.03.013
バッファーによる抗体測定結果の違いおよび阻害試験による測定結果の正確性と信頼性の検証
抗体アッセイの結果は、使用したバッファー系によって大きく異なりますが、これは異なるバッファー成分が異なる非特異的反応に寄与するためです。すべてのタイプの非特異的反応を排除することの重要性を示すために、ヒト血清IgG抗E.coli 抗体および抗CCP抗体を、同じ条件の異なるバッファー系で測定した結果を示します。(下図参照)
なお本稿では、CCPと大腸菌の2種類の抗原を例に挙げておりますが、CCPはRAの診断目的で自己抗原として広く用いられており、また、大腸菌は複雑な表面構造を持つ粒子状抗原であり、血清免疫グロブリンと非特異的に強く相互作用する代表的な抗原として考えられます。また、動物やヒトの消化管に存在する大腸菌は、宿主の免疫系として一貫して相互作用しているため、大腸菌に対する抗体反応は、個体の免疫機能を知る上で貴重なマーカーとなる可能性があります。
Takaki Waritani, Jessica Chang, Bonnie McKinney, Kuniaki Terato(2017), An ELISA protocol to improve the accuracy and reliability of serological antibody assays.
MethodsX: https://doi.org/10.1016/j.mex.2017.03.002
異なるバッファー系を用いた抗E.coli 抗体測定における偽陽性反応と偽陰性反応
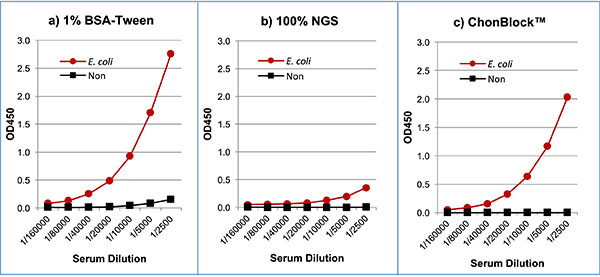
正常ヒト血清をBSA-Tween(a)、100% NGS(b)、ChonBlock™(c)で段階希釈し、抗原未コートウェルとE.coliコートウェルに添加した。
E.coliに結合した抗体は、HRP標識ヤギ抗ヒトIgG(Fc specific)抗体を用いて検出した。
※1%BSA-Tweenバッファー系でもBGノイズOD値は血清希釈率が高いため、本アッセイでは比較的低くなっております。
上図に示すように使用したバッファー系によって希釈曲線の発散が観察されました。1% BSA-Tween(a)ではE.coliでコーティングされたウェルのOD値は、他のバッファー系(bおよびc)よりも有意に高い値を示しました。一方、100% NGSはE.coliに対する抗体の結合を強く阻害しました(b)。このことから、抗E.coli 抗体は100% NGS中の類似抗体によって競合的に阻害されていることが示唆されます。対照的に、ChonBlock™は低いバックグラウンドで明確な希釈曲線を示しました。
異なるバッファー系における測定結果の相違を理解するために、ヒト血清抗E.coli 抗体の阻害試験を、E.coliコートウェルおよび抗原未コートウェルにおいて、1% BSA-TweenおよびChonBlock™を用いて行った結果を下図に示します。1% BSA-Tweenバッファー系では大腸菌による抗体の阻害が約70%であったのに対し(a)、ChonBlock™バッファー系では90%以上の阻害が見られました(b)。これは、BSAが大腸菌粒子と血清免疫グロブリンとの非特異的相互作用を効果的に抑制していないことを示しております。
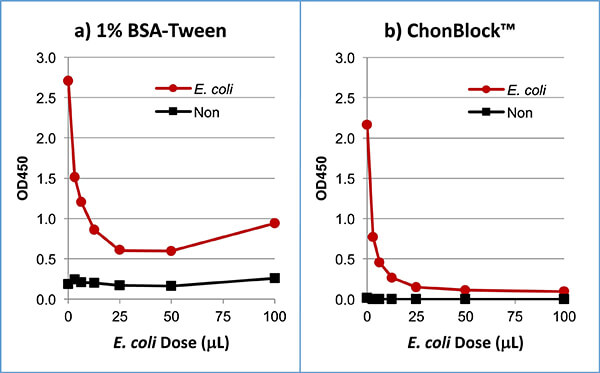
大腸菌懸濁液をマイクロ遠心チューブに分取し、1%BSA-Tween(a)またはChonBlock™(b)で100倍希釈した健常ヒト血清と混合した。4℃一昼夜放置後、抗原未コートウェル(黒線)および大腸菌菌体をコートしたウェル(赤線)に加え、反応させた。ウェルに結合したIgG抗体量をHRP標識ヤギ抗ヒトIgG抗体で測定した。
異なるバッファー系を用いた抗CCP抗体測定における偽陽性反応と偽陰性反応
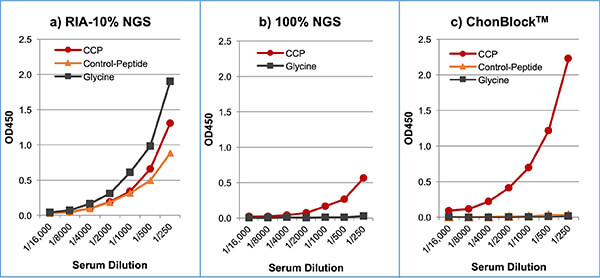
抗原未コート(黒線)、コントロールペプチド(黄線)およびCCPコートウェル(赤線)を、RIA-10% NGS(a)、100% NGS(b)、ChonBlock™(c)でブロッキングした。RA患者血清をブロッキングに用いた各バッファーで系列希釈し、それぞれのウェルに加えた。ウェルに結合したIgG抗体量を、HRP標識ヤギ抗ヒトIgG抗体で測定した。
上図に示すようにChonBlock™では低いBGノイズ反応とともに、高いOD値を示す血清希釈反応曲線が得られました(c)。また、構造的に類似であるが、抗原的には特異的なコントロールペプチドを用いても反応は見られず、抗CCP抗体のCCPに対する特異性の高さが確認されました。一方、第一世代の抗CCP抗体測定の研究報告で用いられたRIA-10% NGSでは、CCP未コート、コントロールペプチドコートおよびCCPコートウェルのいずれにおいても、血清希釈に依存したほぼ同一の反応曲線が得られました(a)。このコントロールウェルが示した高いOD値は、BGノイズによる偽陽性反応とともに、サンプル血清中の抗BSA抗体がブロッキングに使われたBSAと強く反応して生じた偽陽性反応によると考えられます。
さらに、RIA-10% NGSに添加されているNGSの影響を検討するため、100% NGSを用いて抗CCP抗体を測定すると、ChonBlock™が示したOD値と比較し、非常に低いOD値が得られました(b)。この結果からNGSの中にはCCPと共通あるいは類似の抗原エピトープを有する成分が含まれていることが推察され、ヒト血清中の抗CCP抗体とCCPとの反応は強く競合阻害され、偽陰性結果を引き起こすことが示されました。
これらの異なるバッファー系で得られた測定データ間の明らかな相違を検証するために、それぞれのバッファーを用いて阻害試験を行いました。(下図参照) RIA-10% NGSバッファーを用いた場合、CCPによる見かけ上の阻害(約80%)が観察されましたが、抗原未コートのコントロールウェルのBGノイズ値は、抗原コートウェルのOD値よりも高く、阻害試験が成立しませんでした(a)。そのため、市販の抗CCP抗体測定キットに含まれるTriton Xバッファーを使用したところ、Triton XバッファーはBGのノイズ値を有意に減少させましたが、CCPによる阻害は53%しか達成されませんでした(b)。対照的に非特異的なBGノイズ反応を伴わないChonBlock™バッファー系では、ほぼ完全な阻害(92%)が達成されました(c)。
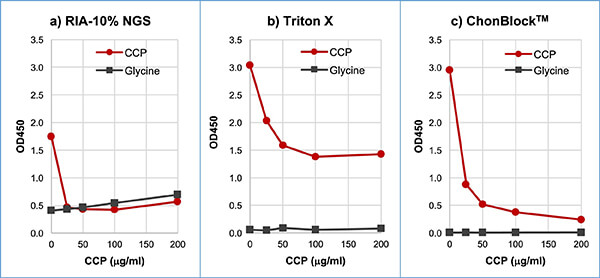
RA患者血清を、RIA-10% NGSバッファー(a)、Triton Xバッファー(b)またはChonBlock™(c)で800倍希釈し、各希釈溶液0.8 mLをCCP溶液(0.1~1 mg/mL)0.2 mLと混和した。4℃で一昼夜放置後、サンプル溶液をグリシン(黒線)およびCCP(赤線)をコートしたウェルにそれぞれ加えた。ウェルに結合したIgG抗体量をHRP標識ヤギ抗ヒトIgG抗体で測定した。
以上の結果からバッファーの選択により、その測定結果にBGノイズ反応と同様、抗原と血清中の免疫グロブリンとの非特異的な相互作用による偽陽性反応が含まれていることが明らかとなりました。一方で、ChonBlock™は血清サンプル中の免疫グロブリンと抗原との非特異的結合による偽陽性反応を効果的に抑制することが示されました。
血清学的抗体測定のための間接ELISA法は、その基礎となる原理の完全な意味合いを理解することなく、あまりにも長い間使用されてきました。結果の誤解や不正確なデータに基づく結論の流布を防ぐためには、プロトコルの変更が必要です。Chondrex社は新しいバッファーシステムであるChonBlock™を開発することで、ELISAの理解を深め、あらゆる研究分野での有効性を向上していきたいと考えています。
